Инженерный путь нейроимпланта: от компьютерной модели до пациента
с помощью нейросети
Мы привыкли считать зрение функцией глаз. Но на самом деле глаза — только сенсоры, преобразующие световые волны в электрические импульсы. Ключевой компонент системы — обрабатывающий их «процессор» — расположен в затылочной части мозга. Можно ли к нему «подключиться», минуя зрительный нерв, и передать импульс напрямую? Еще в начале века это была лишь смелая гипотеза, но со временем она эволюционировала в перспективную технологию. Однако ее внедрение в медицину и сегодня остается сложной задачей.
О том, как развивается это направление, рассказывает биоинженер, офтальмолог и разработчик российского кортикального импланта ELVIS V Андрей Демчинский.
- через какие этапы развития проходит технология и с какими вызовами сталкиваются разработчики
- что сложнее для инженера: «читать» мозг или загружать в него информацию
- как видит пациент с имплантом и как из вспышек света формируется функциональное зрение
Мозг один, подходов много: ключевые различия нейротехнологий
Когда меня спрашивают, чем я занимаюсь, и слышат в ответ о нейроимплантах, многие вспоминают Илона Маска и Neuralink. Ассоциация понятна: компания Маска стала заметной медийной историей в современном мире нейротехнологий. Вот только наш проект ELVIS V ошибочно сравнивают с ее разработкой, известной как brain-computer interface (BCI) или интерфейс «мозг — компьютер».
BCI — это технология «чтения» мозга. Она регистрирует электрическую активность нейронов, выделяет устойчивые паттерны и преобразует их в сигналы, которые используются для управления курсором на дисплее, синтезатором речи или протезом.
Как это происходит технически, я расскажу ниже. Сначала поясню, что «записывать» информацию в мозг значительно сложнее, чем «читать». Хотя бы потому, что при регистрации его активности достаточно корректно распознать уже выявленный нейронный паттерн, а при стимуляции нужно точно знать, куда и как подать сигнал, чтобы мозг воспринял его именно как зрительный, а не как звуковой или болевой.

У Маска есть и другой проект, Blindsight. Его логичнее сопоставлять с ELVIS V: в обоих случаях речь идет о кортикальных нейроимплантах, стимуляции зрительной коры и попытке вернуть зрение людям, его утратившим. Однако открытой технической информации о Blindsight немного. Известно, что разработка получила один из регуляторных статусов Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), который открывает путь к клиническим исследованиям. ELVIS V в России находится примерно на том же этапе — мы здесь, как минимум, не отстаем.
Импланты в офтальмологии: от глаза к затылку
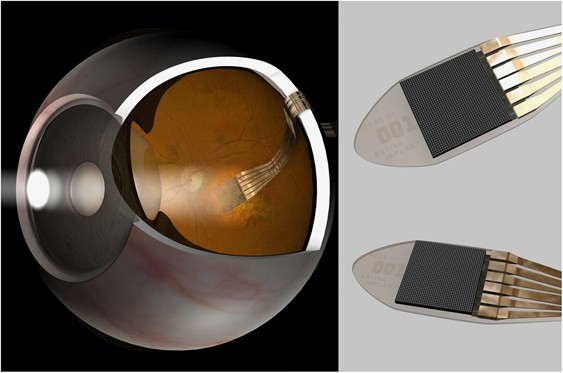
Первыми зрительными имплантами в офтальмологии стали не кортикальные, а ретинальные. Их монтируют на сетчатку, то есть заднюю стенку глазного яблока. Такой подход работает при заболеваниях, когда повреждается лишь один слой ее клеток с фоторецепторами, которые поглощают фотоны и трансформируют свет в понятный мозгу электрический сигнал. Самое распространенное такое заболевание называется пигментный ретинит. Оно врожденное и вызывает постепенное разрушение фоторецепторов.
Десять лет назад в мире существовали три сертифицированных ретинальных системы: американская Argus II, французская Pixium Vision и немецкая Alpha AMS. Последнюю я бы особо выделил за элегантность инженерного решения. Немецкий имплант из 1 600 автономных электродов устанавливали субретинально — под внутренним слоем сетчатки. Каждый электрод имел фоточувствительный элемент, усилитель и стимулятор. Такая конструкция позволяла стимулировать нейроны там, куда попадал свет, и делать это без дополнительных устройств, в то время как Pixium Vision и Argus II требовались специальные очки.
Но с точки зрения анатомии все три системы работали по одному принципу: у пациента стимулировались оставшиеся неповрежденными биполярные и ганглиозные клетки, после чего сигнал шел по зрительному нерву в мозг, как и у здорового человека.
Современное решение: кортикальные импланты
Современные кортикальные импланты можно разделить на две крупные категории.
Первая — пенетрирующие, то есть проникающие, игольчатые.
Такие системы представляют собой матрицу с массивом микроигл из проводящего поликремния, который сочетает в себе жесткость и биосовместимость. Иглы вводятся непосредственно в ткань мозга и воздействуют на нейроны.
Приведу пример: электродная система Utah Array, разработанная в Университете Юты. Ее микроиглы погружаются в кору на глубину 1−2 мм, позволяя регистрировать активность отдельных нейронов или стимулировать их с высокой точностью.
Именно эта точность, а также малая площадь контакта электродов с тканью кортекса и сделала метод настолько распространенным. Сегодня его применяют большинство инженерных команд, работающих в области нейроинтерфейсов.

Однако у иголок есть два серьезных недостатка. Первый очевиден и неспециалисту — они повреждают мозг, пусть и делают это на микроуровне. Второй проистекает из первого: травмированные области быстро рубцуются.
В мозге «латателем дыр» выступает глиальная ткань, то есть биологический диэлектрик, который постепенно экранирует сигнал от электрода. Какое-то время можно компенсировать этот эффект повышением уровня тока. В начале процесса он позволяет «пробить» нарастающую преграду, но рано или поздно электроды всё равно выходят из строя. И чем меньше площадь контакта, тем быстрее это происходит.

Вторая категория — поверхностные электроды.
Здесь речь уже не о жесткой кремниевой матрице с проникающими микроиглами, а о тонкой гибкой пленке с платиновыми контактами, которую размещают на поверхности зрительной коры. Она не повреждает ткань мозга, а аккуратно прилегает к ней. Стимуляция проводится малыми токами, без механического проникновения.
Есть у поверхностного электрода и другое принципиальное преимущество, связанное с анатомией зрительной системы. Область коры, отвечающая за центральное зрение — то самое, которое позволяет нам читать, различать лица и фокусироваться на деталях, — преимущественно расположена на медиальной поверхности мозга, в щели между полушариями. Это анатомически сложная зона, и использование проникающих электродов здесь крайне затруднено. А гибкий пленочный имплант можно аккуратно разместить в межполушарной щели и обеспечить стимуляцию нужной области.
Поэтому при разработке нейроимпланта ELVIS V наша команда сделала выбор в пользу поверхностных электродов. Мы исходили из конкретной задачи по восстановлению функционального зрения у ослепших людей. По этой причине изначально проектировали систему не как лабораторный образец, а как практичное медицинское устройство.
Работа над проектом ведется с 2019 года, и за эти семь лет концепция прошла через несколько инженерных итераций. Сейчас ELVIS V находится на стадии доклинических испытаний.
Как устроен кортикальный нейроимплант ELVIS V: от камеры до фосфена
Система, которая сейчас проходит испытания на приматах, состоит из внешней и внутренней частей. Внешняя представляет собой обруч с камерами и сенсорами, которые анализируют окружающее пространство. Они объединены с микрокомпьютером, который обрабатывает изображение и преобразует его в управляющий сигнал для кортикального импланта — внутренней части системы.

В этой цепочке задействовано несколько алгоритмов на основе искусственного интеллекта, в том числе машинное зрение. Это может показаться избыточным, ведь если мы всё равно не можем передать мозгу детализированную картинку, то зачем столь сложная обработка?
Ответ прост: отсечь информационный шум. Машинное зрение не потребуется пациенту с нейроимплантом, если он пойдет по тихой малолюдной улице. Контуры людей и объектов в такой спокойной ситуации будут считываться ясно. Да, изображение грубое, схематичное, но распознаваемое. А теперь вообразите себе большой проспект или метро в час-пик, когда навстречу двигается поток людей. В какой-то момент визуальный шум станет настолько сильным, что пациент потеряет ориентацию.
Именно тогда и потребуется машинное зрение. Система должна в реальном времени выделить ключевой объект — человека впереди — и отсечь всё второстепенное. В данном случае мы говорим уже не только про трансляцию изображения, но и про осмысленную фильтрацию реальности.

После обработки данные передаются на приемную электронику, которая фиксируется на затылке пациента под кожей. А от нее сигнал поступает уже на матрицу электродов, расположенную под твердой мозговой оболочкой на поверхности зрительной коры. В ответ на ее стимуляцию человек видит фосфены — световые вспышки.
Спираль, а не прямая: тернистый путь нейроимпланта в медицину
Внедрение любой технологии в медицине — процесс полный неожиданностей и инженерных приключений, это не прямая от идеи к клинике, а скорее спираль, где каждый виток может вернуть тебя назад к пересборке конструкции и пересмотру допущений. Но условно всю работу над медицинскими проектами подобного рода можно разделить на четыре этапа.
Этап первый: компьютерное моделирование
В научном мире этот этап еще называют in silico, то есть «в кремнии», с применением программных вычислений. Мы создаем форм-фактор и моделируем «в цифре» электрод, его материалы, параметры тока, рассчитываем распределение электрического поля и взаимодействие с идеализированной моделью коры головного мозга.
На этом же этапе определяются пороги безопасной стимуляции: ограничения закладываются в систему так, чтобы устройство физически не могло нанести повреждение ткани. Это самый быстрый этап и самый «чистый», потому что здесь еще нет биологии, способной преподнести сюрпризы.
Этап второй: тесты на клеточных моделях
Эту стадию разработок в медицине именуют in vitro. Здесь мы оцениваем биосовместимость, то есть то, как живая ткань реагирует на инородный материал. Функциональность на этой стадии, к сожалению, проверить еще невозможно — клетки не образуют органа и не воспроизводят сложную нейронную динамику. Но мы можем увидеть, вызывают ли наши материалы воспалительную реакцию или деградацию клеток.
Этап третий: эксперименты на грызунах
Задача здесь базовая — подтвердить сам факт биологического ответа на стимуляцию: движение лапки грызуна, подергивание его усиков. Это первый момент, когда ты видишь, что электрический импульс действительно преобразуется живой биологической системой в действие.
Этап четвертый: исследования на приматах
Здесь начинаются настоящие сложности. Обезьяне ведь нельзя объяснить эксперимент словами, но при этом, в отличие от грызуна, от нее требуется активное соучастие. Для этого необходимо сформировать условный рефлекс.
Как это делается? Животное сидит перед сенсорным экраном в прозрачном кубе, при этом может свободно двигаться и просовывать руки через отверстия. На экране появляются вспышки и геометрические фигуры, и обезьяна постепенно учится реагировать на них определенным образом. По сути, она запоминает соответствие между зрительным образом и действием.
После хирургической операции и установки импланта эксперимент меняется: свет выключается, и вспышки на экране заменяют на электрическую стимуляцию. Теперь они возникают уже в голове примата — как фосфены. Если обезьяна выполняет правильное действие, мы понимаем, что стимуляция интерпретирована мозгом как зрительный сигнал. Принципиальный момент, потому что именно это и является подтверждением работоспособности всей цепочки.
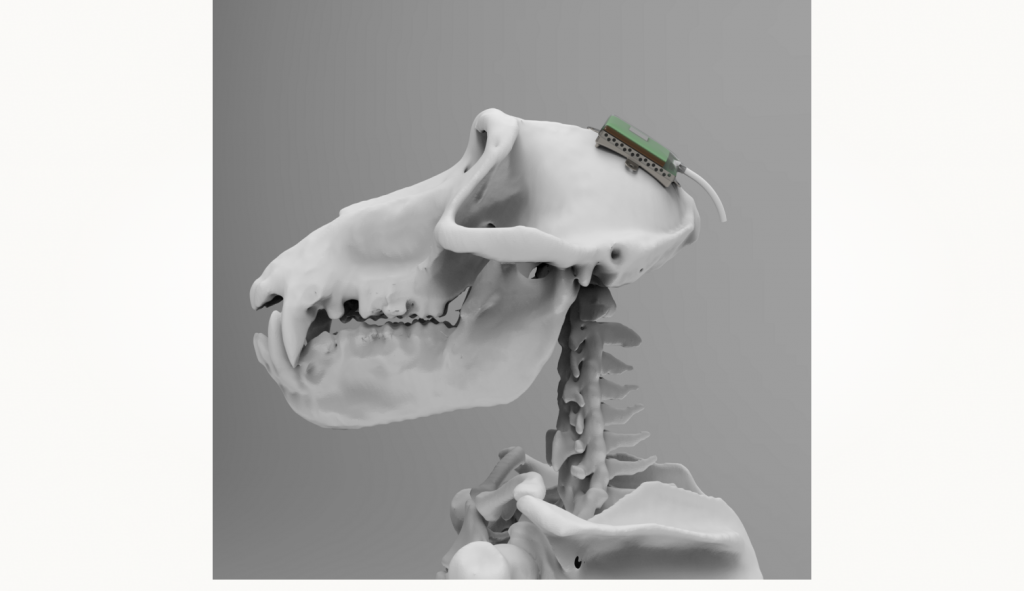
Сейчас мы находимся именно на этом этапе. Работа с приматами продолжается уже около четырех лет. За это время мы успели пройти пару итераций конструкции, каждый раз получая полезные эмпирические данные и улучшая имплант.
Этот этап важен еще и потому, что у нас появляется знание, которого нет в научных статьях. Например, как агрессивные биологические жидкости — ликвор и кровь — проникают внутрь импланта. Какие материалы разрушаются быстрее, как меняются характеристики системы через месяцы.
Этап пятый: клинические испытания
Пройти этот этап нам еще предстоит. Документы на клинические испытания мы планируем подать в 2026 году, а сами испытания могут начаться в 2027-м.
Участниками станут люди с полной потерей зрения. Предварительный возрастной диапазон составит от 20 до 50 лет, а ключевое условие: причина слепоты не должна быть связана с повреждением зрительной коры. Кроме того, у пациентов должно быть минимальное количество тяжелых сопутствующих заболеваний, способных повлиять на состояние мозга.
Сами клинические испытания займут примерно один-два года. И возможно, одного цикла окажется достаточно. Здесь я позволю себе осторожный оптимизм.
На сегодняшний день единственный проект с завершенным циклом клинических испытаний кортикального зрительного импланта — американский Orion, разработанный компанией Second Sight, позднее переименованную в Cortigent.

В 2018 году компания имплантировала шести незрячим пациентам свои устройства и, по данным пятилетнего наблюдения, испытуемые стали видеть лучше. Однако компания столкнулась с финансовыми трудностями и прошла через серьезную реорганизацию. Теперь дальнейшая судьба программы остается неопределенной.
Этот пример хорошо показывает: в нейротехнологиях научный результат и коммерческая устойчивость — две разные задачи, и обе одинаково сложны.
Как я оказался в нейротехнологиях
Сразу скажу: нейротехнологии требуют особого склада ума. Например, способность мыслить на стыке дисциплин, выходить за пределы собственной специальности. Необходимо разбираться в смежных областях, таких как хирургия, физиология, материаловедение, дизайн, инженерия и программирование. В России нейротехнологиями занимаются всего несколько компаний — «Моторика», «Нейри», «Нейроимпланты Элвис» и ряд небольших исследовательских групп.
Мой путь в эту область не был прямым. Я вел колонки об инновациях в офтальмологии, разбирал научные статьи, писал о новых технологиях, и в какой-то момент меня заметили. Предложили участие в одном проекте, затем в следующем. Так постепенно я оказался внутри нынешней команды, где особенно нужны были люди, способные совмещать роли.
Но это не про дар свыше, а способности видеть систему целиком и быстро находить рабочий компромисс.
При этом важно понимать, что развитие такого проекта не бывает ни стремительным, ни легким, и результат не гарантирован. Объективно это одна из самых сложных областей современной медицины и инженерии. Ни одна из существующих в мире систем кортикального зрительного импланта пока не стала массовым продуктом.
Но именно здесь, на стыке инженерии и фундаментальной науки, формируются технологии, которые через десять-двадцать лет могут изменить жизнь миллионов людей. В надежде на это и заключается главный смысл моей работы.